
-
中文 | EN

中文 | EN
发布时间:2021-05-31 00:00:00.0
受体丝氨酸/苏氨酸受体激酶 1(RIPK1)在炎症和细胞死亡过程中扮演着重要角色。Nec-1s 是特异性抑制 RIPK1 激酶活性的小分子化合物。在过去十余年的研究中,RIPK1 的激酶活性在程序性坏死 necroptosis 过程中发挥的作用已被研究较多,而我们的研究则关注 RIPK1 激酶活性目前知之甚少的另一方面——在细胞不发生死亡的情况下在TLR信号通路中调控细胞炎症因子产生的作用机制。
近期,中科院上海有机化学研究所生物与化学交叉中心袁钧瑛课题组在小胶质细胞系BV2 细胞和原代星形胶质细胞中发现,RIPK1可被LPS/zVAD 诱导而激活,在激酶激活后不引起细胞死亡,转而调控 NF-κB 通路依赖的细胞炎症因子的产生。更重要的是,RIPK1在调控炎症因子中的作用呈现双重不同动力学的特点:在信号通路的早期阶段,RIPK1对炎症因子的调控需要其支架功能而不需要激酶活性;而在信号通路的晚期阶段,RIPK1同时需要支架功能和激酶活性来共同调节下游炎症因子的产生。
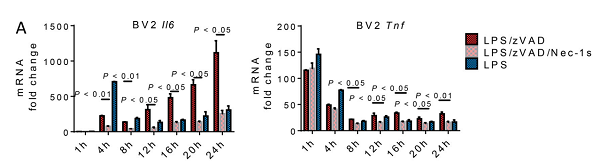
图1.RIPK1激酶活性在后期阶段调控炎症因子的产生
进一步研究发现, LPS/zVAD 诱导产生的TNF-α 自分泌对于该通路中RIPK1 激酶的激活具有重要作用。同时,我们也利用质谱检测技术发现,激活的RIPK1与 FADD,Caspase-8 等关键蛋白组织形成一个新型复合物。该复合物也同时包含了多种经典 NF-κB 通路蛋白,且受 RIPK1 激酶活性控制,其中,FADD和Caspase-8 是该种新型调控机制中的重要蛋白。RIPK1的激酶活性可影响其与FADD和Caspase-8等关键蛋白的相互作用,进而调控下游 NF-κB 通路依赖的细胞炎症因子的产生。因此我们的研究证明了RIPK1的激酶活性可以通过影响其支架功能来发挥作用。
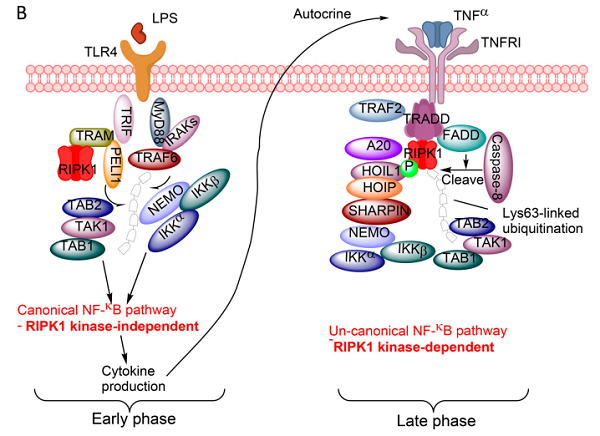
图2. RIPK1在TLR信号通路中双重调控炎症反应的模式图
由于LPS/zVAD处理可以用来模拟细胞受到病原体侵染并抑制Caspase活性的病理条件,因此我们的研究不仅揭示了RIPK1 激酶活性影响炎症因子表达的新功能,以及 RIPK1 激酶依赖性的炎症反应的调控通路,而且为 RIPK1 激酶抑制剂用于治疗炎症疾病提供了有利线索。该研究得到了国家自然基金的大力支持。相关工作发表于Journal of Cell Biology。
该论文的通讯作者为袁钧瑛研究员,第一作者是中科院上海有机化学研究所生物与化学交叉研究中心的黄心悦博士。
