
-
中文 | EN

中文 | EN
发布时间:2021-06-30 00:00:00.0
帕金森病(Parkinson’s disease,PD) 是仅次于阿尔茨海默病的第二大神经退行性疾病。PD病人大脑黑质中,α-突触核蛋白(α-synuclein,α-syn)聚集形成的淀粉样病理纤维为主要成分的路易小体是PD的重要病理学特征。α-Syn病理纤维一旦形成,不仅能够在脑中神经元之间传播,还能够从肠道传播入脑。在传播过程中,其能高效诱导非聚集态的内源α-syn形成具有传播性的病理纤维。α-Syn病理纤维的传播和扩散与PD病情发展密切相关。然而,为什么α-syn只有在形成纤维以后才具有传播性?α-Syn纤维如何在细胞间传播?这些尚未解决的问题对于理解PD的发病机制以及药物研发至关重要。
近日,中国科学院上海有机化学研究所刘聪课题组与清华大学李艳梅课题组,美国约翰霍普金斯大学毛晓波课题组及Ted Dawson课题组合作揭示了受体介导的α-syn病理纤维在细胞间传播的分子机制。相关的工作于6月29日在PNAS上在线发表。
研究者利用纳米金颗粒标记和生物膜层干涉技术(bio-layer interferometry, BLI)发现膜表面受体LAG3(lymphocyte activation gene3)的D1结构域(L3D1)可以特异性的识别α-syn纤维,L3D1与α-syn纤维的结合力是其与α-syn单体结合力的~200倍。核磁共振(NMR)研究表明L3D1利用其带有正电荷的结合口袋识别α-syn带有负电荷的C末端。HADDOCK、分子动力学模拟及突变实验进一步证明静电相互作用在L3D1和α-syn的特异性识别中其中起主导作用。研究者进一步运用PRE和BLI等技术方法发现a-syn在单体状态下其C末端与其它区域(N末端及中间的纤维形成核心区)存在长程弱相互作用(图1),这使得a-syn的C末端在单体状态下以动态自锁的形式存在,不利于其与L3D1的结合。而在纤维状态下,a-syn的 C末端被释放并高度富集在纤维表面,从而显著增强a-syn纤维与L3D1的结合能力(图1)。
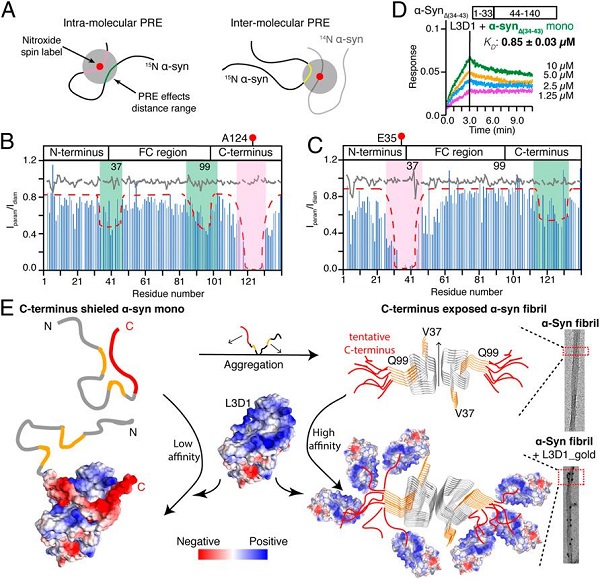
图1:α-syn单体的PRE实验以及L3D1特异性结合α-syn 纤维的分子机制示意图
α-Syn的C末端S129位磷酸化修饰长久以来被作为PD的重要病理标志之一。然而S129磷酸化修饰在PD发病过程中的作用一直没有明确的答案。研究人员通过生物-化学半合成的方法在体外获得了S129位磷酸化修饰的高纯度a-syn蛋白 (pS129 a-syn),并发现S129位磷酸化不但能够极大地提升α-syn纤维与受体蛋白之间的结合力,还能够加速α-syn纤维在神经元中的内吞、聚集和传播,增强α-syn纤维的神经毒性,并加重小鼠模型中的PD相关症状。
本研究还发现受体蛋白淀粉样前体样蛋白-1(amyloid precursor-like protein 1, APLP1)的E1结构域,同样会利用其蛋白表面的正电荷口袋结合α-syn纤维负电荷富集的C末端,而S129位磷酸化同样会增强其与α-syn纤维的结合能力。这暗示着α-syn病理纤维运用其C末端与不同的受体蛋白结合,进而介导其在细胞间的传播。
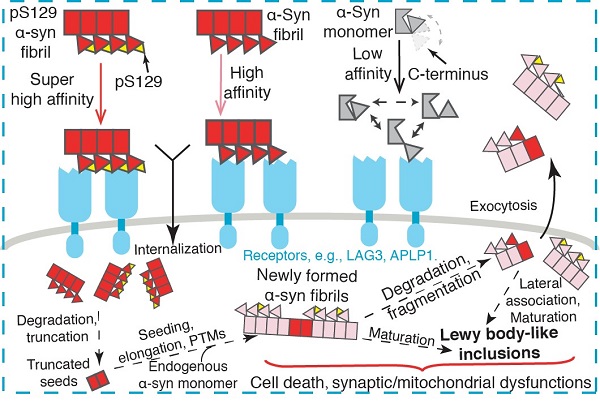
图2:受体介导的α-syn病理纤维传播示意图
综上,本工作研究了膜受体介导的α-syn病理纤维在细胞间传播的分子机制。首次发现α-syn的C末端作为α-syn病理纤维传播的关键区域,通过结合不同膜表面受体蛋白的正电口袋,介导α-syn病理纤维进入到细胞中,诱导细胞内源非聚集态的α-syn病理性聚集,并引发相应的细胞毒性和死亡等(图2)。在生理状态下,α-syn的C末端被其自身的其他区域所屏蔽而处于自锁状态;而在病理条件下,α-syn单体形成纤维,其C末端被释放并富集在α-syn纤维的表面,从而增强α-syn纤维与受体蛋白的结合。本工作阐明了受体蛋白介导的α-syn病理纤维传播的分子机制,加深了对α-syn病理纤维传播,尤其是S129位磷酸化在其中作用的理解。同时,提出α-syn与受体蛋白之间的作用界面可以作为潜在的抗PD药物筛选的靶点,为PD药物的设计和研发提供了新的思路。
