
-
中文 | EN

中文 | EN
发布时间:2021-09-09 00:00:00.0
2021年9月9日,中国科学院上海有机化学研究所生物与化学交叉中心刘聪课题组与武汉大学梁毅课题组合作成果在Science Advances上在线发表,题为:Genetic prion disease–related mutation E196K displays a novel amyloid fibril structure revealed by cryo-EM。该工作利用冷冻电镜技术解析了全长朊病毒蛋白家族遗传病理性突变体E196K蛋白纤维的近原子分辨率结构,发现了E196K突变通过破坏野生型朊病毒蛋白病理纤维中的关键相互作用力,导致了纤维结构的重排,进一步揭示了不同朊病毒蛋白病理突变体聚集多态性的分子机制。
Prion疾病是一类由朊病毒蛋白(prion protein, PrP)发生错误折叠,聚集形成致病性的朊病毒(PrPSc)导致的具有高致死率的神经退行性疾病,该疾病可在多种动物包括人类之间传播。其病理特征主要为细胞中具有正常构象的朊蛋白(PrPC)发生错误折叠形成病理型的朊病毒蛋白(PrPSc)。Prion疾病分为散发性、家族遗传性和感染性三种类型,家族遗传性prion疾病的发生与朊蛋白基因的突变密切相关。已发现引起家族遗传性prion疾病的PrP突变位点共33个,包含42种不同氨基酸的突变。这些不同的病理突变体可以形成多种不同的朊病毒株型,引发不同的临床症状,导致不同疾病的发生,如克雅氏病(Creutzfeldt-Jakob disease, CJD)、致死性家族失眠症(fatal familial insomnia, FFI)和格斯特曼氏综合征(Gerstmann-Sträussler-Scheinker disease, GSS)等。然而,病理性突变体是如何改变朊病毒蛋白结构的?不同的朊病毒蛋白病理性突变体如何引起不用的病理临床症状?这些都是领域内尚未解决的重要科学问题。
在本研究中,研究人员对克雅氏病(CJD)家族性突变位点E196K进行研究。研究人员制备了高度均一、分散的全长人源朊蛋白病理突变体E196K淀粉样纤维,并进一步运用冷冻电镜技术在近原子水平上解析了E196K纤维的高分辨率冷冻电镜结构(3.04 Å)。研究发现,E196K突变破坏了野生型朊病毒纤维中的关键相互作用力,导致了纤维纤维结构的重排,形成了与野生型朊病毒纤维完全不同的结构。该结构由两根原纤维以左手螺旋的方式缠绕而成,纤维核心宽度约为11 nm,半螺旋周期为126.4 nm(图1)。
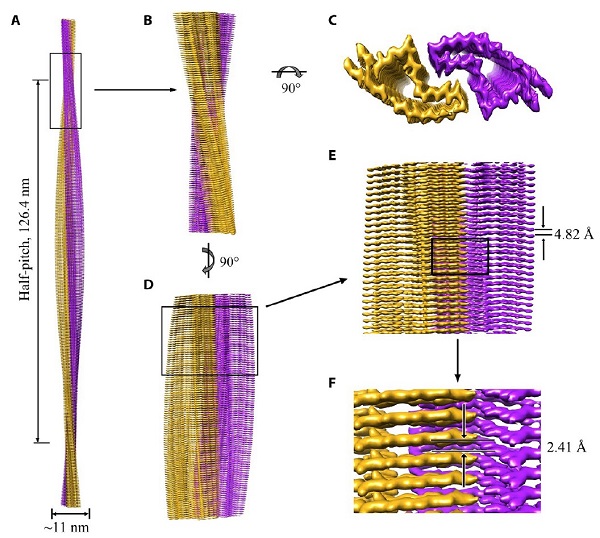
图1:E196K纤维冷冻电镜结构
研究人员进一步发现E196K纤维核心主要由其C端的175-217组成,包含5个β-折叠结构。在E196K纤维结构中,来自两个亚基的Lys194、Lys196、Glu200和Glu207组成四对盐桥,形成了一个同时包含亲水氨基酸和疏水氨基酸的锯齿形相互作用界面(图2)。该研究揭示了朊病毒蛋白病理突变体引起聚集纤维多态性的分子机制,为发展相关诊断和治疗手段提供了分子基础,具有较为重要的科学意义。
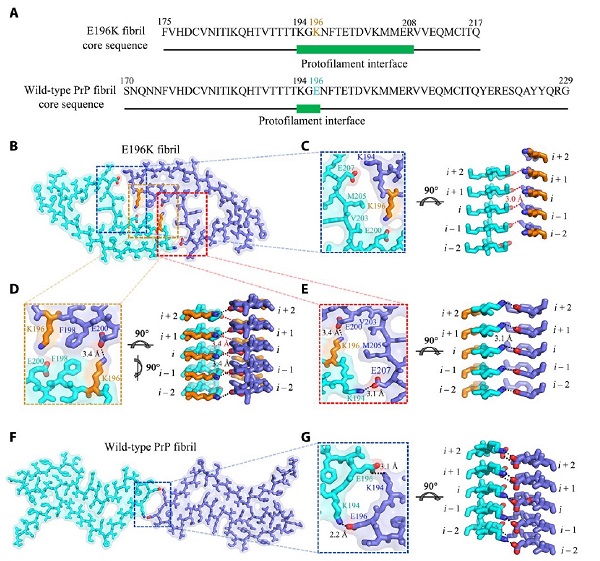
图2:E196K纤维与野生型纤维的结构对比
上述工作由中科院上海有机所生物与化学交叉研究中心刘聪研究员和武汉大学梁毅教授为共同通讯作者,梁毅课题组博士王利强和刘聪课题组博士研究生赵焜以及梁毅课题组博士研究生袁菡烨为共同第一作者。研究经费主要来自国家自然科学基金委和国家科技部的资助。
Researchers elucidate the molecular mechanism of the diverse prion strains
Recently, a research paper titled “Genetic prion disease–related mutation E196K displays a novel amyloid fibril structure revealed by cryo-EM” was published on the Science Advances journal by Prof. Cong Liu from the Shanghai Institute of Organic Chemistry, Chinese Academy of Sciences, in collaboration with Prof. Yi Liang from Wuhan University.
Prion diseases are infectious, fatal neurodegenerative diseases primarily caused by the conformational conversion of prion protein (PrP) from its cellular form (PrPC) into a protease-resistant, aggregated form (PrPSc). Forty-two different mutations in the PrP gene (PRNP) were identified to cause a variety of genetic prion diseases, including genetic Creutzfeldt-Jakob disease (CJD), Gerstmann-Sträussler-Scheinker disease, and fatal familial insomnia. However, the roles of disease-related mutations play in prion fibril structure and the molecular mechanism of the diverse prion strains are still unknow.
In this paper, researchers obtained homogeneous amyloid fibrils in vitro from recombinant, full-length human E196K PrP and determined the near atomic structure by using cryo-EM. The results showed that the E196K mutation disrupts key interactions in the wild-type PrP fibril, forming an amyloid fibril with a conformation distinct from the wild-type PrP fibril. This study elucidates the molecular mechanism of the diverse prion strains and sheds light on the development of new strategies and targets for diagnosis and treatment of diseases.
